Comment Calculer La Masse Molaire D Un Polymère
| | polym�re; chlorure de vinyle ; amine ; craquage du butane ; solvant chlor�southward ; alcools En poursuivant votre navigation sur ce site, vous acceptez l'utilisation de Cookies vous proposant des publicit�s adapt�es � vos centres d'int�r�ts. |
| | |
| | United nations polym�re a pour masse molaire moyenne eight,75. 10 4 k/ mol et pour degr� de polym�risation moyen environ n=1,four. x3. Son analyse chimique montre qu'il contient, en masse, 56,8 % de chlore 38,4 % de carbone et le reste d'hydrog�ne.
corrig� Masse molaire du monom�re = eight,75. 10 4 / ane,four. 10iii = 62,5 g/mol. formule fauna CxHyClz. masse molaire 12 ten +y +35,five z= 62,5 en cons�quence z ne peut �tre sup�rieur � 1. % hydrog�ne = 100-38,4-56,8=4,8 % 12 x / 38,four = y / 4,8 = 35,5 z / 58,half-dozen = 62,five / 100= 0,625 x= 0,625*38,4/12 = 2 ; y = 0,625*four,eight = 3 ; z= 0,625*58.6/35.5=1 CiiHiiiCl chlorure de vinyle ( monom�re) -[CHtwo-CHCl]- n fois polychlorure de vinyle ( polym�re) En 1913, d�but de la production industrielle de PVC par le proc�d� en �mulsion. En 1914, Klatte d�pose le brevet de fabrication du chlorure de vinyle par r�action entre l'ac�tyl�ne et le chlorure d'hydrog�ne. Au d�but des ann�es 1930, la production industrielle du PVC appara�t. combustion du monom�re : C2H3Cl + ii,5Oii --> 2 COtwo + HiiO + HCl Le gaz d'odeur piquante est du chlorure d'hydrog�ne HCl, tr�s soluble dans fifty'eau, il donne une solution d'acide chlorhydrique. (mesurer le pH de la solution ou v�rifier que la solution est acide avec un papier indicateur universel) masse molaire chlorure de vinyle : 62,five g/mol Qt� de mati�re chlorure de vinyle (mol) = masse (chiliad) / masse molaire (thousand/mol) n (chlorure de vinyle)= 1,5 xeleven/62,5 = 2,4 10nine mol n( HCl) = 2,4 x9 mol masse HCl (thousand)= Qt� de mati�re (mol) * mase molaire HCl (g/mol) = 2,4 109*36,v = 8,76 10ten g = eight,76 ten4 t. |
| | L'analyse d'une monoamine est r�alis�eastward par combustion de 150 mg d'amine.On obtient 355,six mg de dioxyde de carbone et 205 mg d'eau. L'�l�ment azote se retrouve sous forme de diazote gazeux : le volume recueilli sous 98,66 kPa, � 20 �C est 31,v mL.
d'o� n( amine) = ii northward( Northtwo) volume molaire des gaz : 5= RT/P = 8,31 * (273+xx) / ix,866 teniv = 2,47 x-two m3 /mol= 24,7 L/mol north(Northwardii ) = volume diazote (L) / volume molaire (L/mol) = 31,v x-3 / 24,vii = 1,275 10-3 mol n(amine) = ii*1,275 x-iii = two,55 10-3 mol Qt� de mati�re amine (mol) = masse (1000) / masse molaire (thousand/mol) soit M = masse /n(amine ) M= 0,15 / two,55 10-iii = 59 g/mol Thousand= 12 x + y + 14 = 59 soit 12 ten+y = 45 ten= 3 et y = 9 CHthree-CH2-CH2-NH2 : propylamine (CH3)2CH-NHtwo : isopropylamine Une amine a des propri�t�south basiques. |
| | Le craquage catalytique du butane gazeux est effectu� � 500�C sous une pression de v,0.10five Pa. On obtient un m�lange de 2 hydrocarbures gazeux appel�s A et B. Une solution de permanganate de potassium en milieu basique devient verte en pr�sence du compos� B et reste violette en pr�sence du compos� A. Afin de d�termin� la formule B, on fait agir sur lui une solution aqueuse de dibrome. Une masse m(B) de 0.70g de B suffit pour d�colorer une solution aqueuse contenant m(Br2)=iv.0 g de dibrome. Le compos� A subit une d�shydrog�nation catalytique et se transforme en un compos� C qui se comporte comme B vis-�-vis d'une solution de permanganate de potassium en milieu basique. Le compos� B subit une r�action de polyaddition et forme united nations polym�re de degr� de polym�risation n=1,0.teniii.
corrig� Le test avec le permanganate de potassium indique que 50'hydrocarbure b est insatur� : ( alc�ne de formule animate being CnH2n) B+Br2 = B Brii dibromoalcane Qt� mati�re dibrome : 4/160 = 0,025 mol Qt� mati�re B : 0,7 /G =0,025 mol d'o� M= 0,seven/0,025 =28 B est �thyl�ne C2H4. craquage du butane : C4H10 --> C2Hiv +C2H half dozen ( �thane) d�shydrog�nation �thane : C2H 6 --> C2H4 + H2 polym�risation de l'�thyl�ne : north CC2H4 -->-[-CHtwo--CH2]- n fois poly�thyl�ne masse molaire du polym�re : 1000 * 28 = 28 000 g/mol. |
| | Un polym�re obtenu par polyaddition a pour masse molaire moyenne M = 47 040 g/mol et pour indice de polym�risation n = 1120 . Une analyse �l�mentaire du monom�tre montre qu'il contient en masse 85,7 % de carbone et fourteen,3 % d'hydrog�ne.
corrig� masse molaire du monom�re = Thou/due north = 47040/1120 = 42 1000/mol formule brute du monom�re CxHy ; 12 ten / 85,7 = y / fourteen,3 = 42/100 = 0,42 10 = 0,42*85,7/12 =three ; y = 0,42*14,iii =6 CH3-CH=CHii prop�ne. polym�risation : nCHiii-CH=CHtwo --> -[-CHiiiCH--CHii-]- north fois polym�re |
| | United nations compos� chimique B ne contient que des atomes de C, H et O. Une solution aqueuse dilu� de B fait rougir l'h�lianthine. Le dosage de v,0 mL de cette solution aqueuse, de concentration massique eight,4g.Fifty-1, north�cessite 7,0 mL d'une solution de soude � 0,100mol.50-one.
corrig� si fifty'h�lianthine est rouge, c'est un acide organique. Un acide carboxylique poss�de le groupement -COOH Lors du dosage par la soude on a � fifty'�quivalence : n(acide )=n(OH- )si c'est un monoacide carboxylique. northward(OH- ) =COH-*V�qui = 0,one*7 x-3 = 7 ten-4 mol vii 10-4 mol d'acide dans v mL de solution soit : 7 10-4 / 5 ten-three = 0,14 mol/L . concentration molaire (mol/50) * masse molaire (g/mol) = titre massique (grand/50) d'o� : M= 8,iv / 0,14 = threescore k/mol . Formule creature : CxHyOtwo : 12x / xl = y / 6,67 = M/100 = 0,6 x= 0,6*40/12 =2 ; y = 0,six*6,67 = 4 CiiH4O2 soit CHiii-COOH acide �thano�que au air-conditioning�tique. |
| | On br�le 0,500 m d'un echantillon d'une esp�ce chimique.
corrig� 50'esp�ce chimique est donc seulement compos�due east de Carbone, Hydrog�ne.( hydrocarbure) Le chlorure de calcium anhydre CaCl2 fixe des mol�cules d'eau. La prise de masse stand for � la masse d'eau contenue dans les gaz (ou fum�es) de combustion, soit 643 mg d'eau. Il ne reste que CO2 qui ne r�agit pas avec le chlorure de calcium. La prise de masse correspond � la fixation du COtwo par la solution basique sous forme d'anion carbonate COiii 2-. 2Na+ + 2OH- + COii --> 2Na+ + COthree 2- + H2O Na+ est united nations ion qui north'intervient pas dans le processus( ion spectateur) Quantit� de mati�re ( mol ): masse (1000)/ masse molaire (grand/mol) n(HtwoO) = 0,643/(2+16) = 0,0357 mol n(COii) = one,57/(12+2*16) = 0,0357 mol |
| | Synth�se du chlorure de vinyle en plusieurs �tapes : - on fait r�agir du dichlore sur fifty'�thylene en phase liquide a 50�C et sous une pression de v.105 Pa ; - le compos� 10 obtenu est ensuite chauff� vers 600�C sous une pression de 25.10five Pa, en pr�sence de nickel et de chrome. On obtient du chlorure de vinyle et united nations gaz Y d'odeur piquante tr�due south soluble dans l'eau ; - cascade identifier ce gaz, on proc�de � sa dissolution dans l'eau. La solution obtenue est jaune en pr�sence de BBT et on obtient un pr�cipit� blanc noircissant � la lumi�re par ajout d'une solution aqueuse de nitrate d'argent.
corrig� �thyl�ne + dichlore --> one,2-dichlorom�thane CHtwo=CHtwo+ Cl2 --> CHiiCl-CH2Cl solution aqueuse de nitrate d'argent. Ag+(aq) + NOthree -(aq) : mise en �vidence de 50'ion chlorure Cl-. la couleur jaune du BBT met en �vidence un milieu acide ( ion oxonium H3O+) Y est le chlorure d'hydrog�ne HCl(k) : HCl(g) + H2O = H3O+ + Cl-.( r�activeness acide base) CHtwoCl-CH2Cl --> CH2=CHCl (chlorure de vinyle) + HCl nCH2=CHCl --> --[CH2--CHCl ] --n fois polychlorure de vinyle. |
| | Trois solvants chlor�s sont utilis�s aujourd'hui : le chlorure de yard�thyl�ne ou dichlorom�thane CHtwoCl2, , le trichlor�thyl�ne ClHC= CCl2 et le perchlor�thyl�ne, ou r�trachloro�thvl�ne, Cl2C= CCl2 . Le dichlorom�thane peut �tre pr�par� directement par action du dichlore sur le m�thane ; les deux autres peuvent l'�tre par activity du dichlore sur 50'�thyl�ne H2C= CH2, avec �limination de chlorure d'hydrog�ne selon : Ces trois solvants sont ininflammables et north'affectent pas la couche d'ozone stratosph�rique en raison de leur faible dur�e de vie. La French republic en produit environ 300 mille tonnes par an et en consomme � peu pr�s le tiers.
corrig� 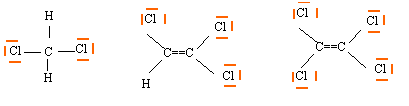 masse molaire CiiCl4 : M= ii*12+4*35,v = 166 thousand/mol Qt� de mati�re (mol) = masse (g) / masse molaire (grand/mol) n(CtwoCl4)= ii,5 108 / 166 = 1,506 106 mol n(C2Hfour)= 2 n(C2Cl4)=three,012 106 mol masse �thyl�ne (g) = masse molaire (g/mol) * Qt� de mati�re (mol) = 28*3,012 tenhalf dozen mol=viii,43 107 g = 84,3 t . n(Clii)= 7 northward(CiiCl4)=1,054 10vii mol volume de dichlore (Fifty) = volume molaire (L/mol) * Qt� de mati�re (mol)= 24*i,054 10seven = 2,53 10 8 50. n(C2HCl3)= north(C2Cl4)=one,506 106 mol masse C2HCl3 (k) = masse molaire (1000/mol) * Qt� de mati�re (mol) = 131,5* 1,506 10half-dozen =ane,98 108 thousand = 198 t . north(HCl)= n(Cl2) = i,054 tenseven mol volume acide chlorhydrique (50) = Qt� de mati�re (mol) / concentration (mol/Fifty)= ane,054 xseven / 11 = 9,58 105 Fifty = 958 m 3 . |
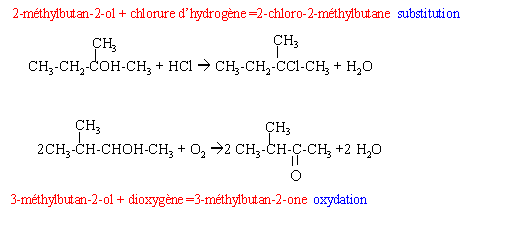
| | Pour chacune des �quations ci-dessous, nommer les r�actifs et les produits, puis indiquer si la r�action associ�due east est une d�shydratation, une substitution, une addition, une oxydation ou une r�duction… CH3-CH=CHtwo + HiiO --> Z Cascade cette derni�re r�action, two isom�res de Z sont envisageables, lequel obtient-on ? corrig� CH3 - CH2 - CHOH - CH3--> CH3 - CH = CH - CHthree + H2O d�shydratation butan-2-ol --> merely-2-�ne ( Z ou E) +eau CH3-CH=CHii + H2O --> CH3-CHOH-CHiii addition prop�ne + eau --> propan-two-ol |
| | Un volume Five=25 mL de cyclohexanol Chalf-dozenH11-OH est agit� avec une solution concentr�e d'acide chlorydrique en exc�due south. April�due south 30 minutes d'agitation, le yard�lange est introduit dans une ampoule � d�canter. La phase aqueuse est �limin�e, puis la phase organique est lav�e avec une solution d'hydrog�nocarbonate de sodium, Na+ + HCO3 -; et enfin trait�e par du sulfate de magn�sium anhydre. La stage organique est filtr�e, puis distill�e ; la masse de distillat alors recueilli vaut thou=25.7g. donn�es : �(cyclohexanol)=0.962g/mL ; �(chlorocyclohexane)=1g/mL; �(phase aqueuse)=i.10g/mL ; Teb(chlorocyclohexane)=142�C ; Teb(cyclohexanol)=161�C
corrig� H+ + HCO3 - = CO2 (g) + HtwoO d�gagement de dioxyde de carbone chlorocyclohexane + Ag+ donne un solide blanc AgCl. Lors de la distillation le chlorocyclohexane, compos� organique le plus volatil , distille vers 142 �C On peut �galement d�terminer sa masse volumique : 1 g/mL masse cyclohexanol(chiliad) = book (mL) * masse volumique ( m/mL) 25*0,962 = 24,05 g M(cyclohexanol)= vi*12+12+xvi =100 g/mol n(cyclohexanol) = 0,24 mol C6Heleven-OH + H+ + Cl- = C6H11- Cl + H2O donc 0,24 mol chlorocyclohexane Chiliad (chlorocyclohexane)=6*12+eleven+35,5 = 118,5 g/mol masse thursday�orique chlorocyclohexane (one thousand): Qt� de mati�east (mol) * mase molaire g/mol) =118,five*0,24 = 28,4 g rendement : masse r�elle(1000) / masse th�orique (thou)=25,7 / 28,4 = 0,9 |
| | On r�alise au laboratoire la d�shydratation du 3,3-dim�thylbutan-1-ol (CH3)3 C-CHtwo-CH2-OH. Apr�s chauffage � reflux pendant trente minutes d'united nations k�lange constitu� de Five = 30,0 mL de cet alcool et de 5 mL d'acide sulfurique concentr�, le grand�lange est introduit dans une ampoule � d�amble. La phase aqueuse est �limin�, puis la phase organique est lav�east avec une solution d'hydrog�nocarbonate de sodium Na+ + HC03 - et, enfin, trait�e par du sulfate de magn�sium anhydre. Le one thousand�lange obtenu est filtr�. On recueille une masse m' = 11,6 g d'un alc�ne A.
Donn�east : �(3,iii-dim�thylbutan-1-ol) = 0,812 g.mL-1. corrig� H+ + HCOiii - = CO2 (m) + H2O on �limine 50'exc�s d'acide sulfate de magn�sium : d�ss�chant, �limine les traces d'eau (CH3)3C-CH=CH2 3,3-dim�thylbut-i-�ne mise en �vidence de l'alc�ne : d�colore l'eau de brome masse alcool (g) = masse volumique (g/mL) * volume (mL)=0.812*xxx =24,36 g mase molaire alcool : M=12*vi + xiv+sixteen = 102 g/mol due north(alcool) = masse (grand) / masse molaire (g/mol) =24,36/102 = 0,239 mol (CHiii)3 C-CHtwo-CHii-OH = (CH3)3C-CH=CH2 +H2O donc d'apr�southward les coefficients de l'�quation : 0,239 mol alc�ne M(alc�ne) = vi*12+12 = 84 m/mol masse alc�ne =masse molaire (thou) * quantit� de mati�re (mol) = 84*0,239 = 20,i one thousand rendement = masse r�elle / masse th�orique = 11,6/20,one = 0,58 ( 58%) |
| | On souhaite determiner la formule brute d'une espece chimique X. United nations �chantillon est brul� en presence d'un exc�due south de dioxyg�ne et de produits de combustion sont r�cup�r�s.On ne trouve que CO2 et H2O.
corrig� les hydrocarbures et les compos�s oxyg�n�s conduisent par combustion au CO2 et � H2O : on ne peut pas donner le nom de la famille � laquelle appartient X. aldehyde : exam positif � la liqueur de Fehling formule brute : CxHyO ; M= 12 10+y+sixteen % massique d'�l�ment oxyg�ne : 100-66,7-11,1 = 22,2 % 12x/66,vii= y/ xi,i = xvi / 22,ii = Chiliad/100 d'o� M= 1600/22,2 = 72 k/mol et 10=4 et y=viii CHiii-CH2-CH2-CHO : butanal CH3-CH(CH3) -CHO : two-m�thylpropanal |
| | |
Comment Calculer La Masse Molaire D Un Polymère,
Source: https://www.chimix.com/an5/prem5/orga.htm#:~:text=masse%20molaire%20du%20polym%C3%A8re%20%3A%201000,indice%20de%20polym%C3%A9risation%20n%20%3D%201120%20.
Posted by: hickmanwelds2000.blogspot.com

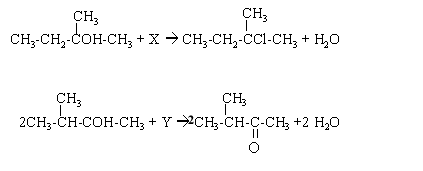

0 Response to "Comment Calculer La Masse Molaire D Un Polymère"
Post a Comment